안녕하세요. 맑은 향기입니다.
중학교 3학년 과학의 첫 문을 여는 '화학 반응의 규칙과 에너지 변화' 단원은 단순히 암기할 내용이 많아 보이지만, 사실은 자연의 정교한 질서를 배우는 아주 매력적인 파트랍니다.
원자와 분자가 춤을 추듯 자리를 바꾸며 새로운 물질을 만들어내는 과정을 이해하면, 우리 주변에서 일어나는 모든 변화가 새롭게 보일 거예요.
오늘 제가 준비한 프리미엄 요약 가이드를 통해 여러분의 과학 실력을 한 단계 업그레이드해 보세요. 복잡한 공식도 아주 쉬운 비유로 풀어드릴 테니 끝까지 집중해 주세요! 이 글만 봐도 이번 단원 정복은 문제없을 거예요.
"눈에 보이지 않는 원자들의 재배열 속에 숨겨진 완벽한 '수학적 레시피'를 찾아낼 준비가 되셨나요?"
1. 물질의 변화: 물리 변화 vs 화학 변화
우리 주변의 변화는 성질의 유지 여부에 따라 크게 두 가지로 나뉩니다. 물리 변화는 '분자의 배열'만 바뀌어 모양이나 상태가 변하는 현상입니다. 반면, 화학 변화는 '원자의 배열'이 완전히 달라져 성질이 전혀 다른 새로운 물질이 생성되는 현상입니다.
| 구분 | 물리 변화 | 화학 변화 |
|---|---|---|
| 핵심 원인 | 분자의 배열 변화 | 원자의 배열 변화 (분자의 종류가 바뀜) |
| 성질 변화 | 물질 고유 성질 유지 | 새로운 성질의 물질 생성 |
| 대표 예시 | 얼음이 녹음, 유리컵 깨짐, 설탕의 용해 | 종이가 탐, 철이 녹슬음, 과일이 익음 |
2. 화학 반응식 나타내는 3단계 방법
화학 반응을 기호로 나타낼 때는 약속된 3단계를 따릅니다. 메테인의 연소 반응을 예로 들어볼까요?
메테인 연소 반응식 3단계
- 1단계: 반응물(왼쪽)과 생성물(오른쪽)을 이름으로 쓰고 화살표로 연결
(메테인 + 산소 → 이산화 탄소 + 물) - 2단계: 각 물질을 화학식으로 전환
(CH4 + O2 → CO2 + H2O) - 3단계: 화살표 양쪽의 원자 종류와 개수가 같도록 계수 맞추기
(CH4 + 2O2 → CO2 + 2H2O)
* 여기서 계수비(1:2:1:2)는 곧 입자 수(분자 수)의 비와 같습니다.
3. 질량 보존 법칙: 변하지 않는 마법
프랑스의 화학자 라부아지에가 제안한 질량 보존 법칙은 화학 반응 전 반응물의 총 질량과 반응 후 생성물의 총 질량은 항상 같다는 법칙입니다.
이것을 레고 블록에 비유해 볼까요? 레고 블록 10개로 자동차를 만들다가, 이를 분해해서 비행기를 만든다고 해도 사용된 레고 블록의 종류와 개수는 10개 그대로죠? 마찬가지로 화학 반응에서도 원자의 종류와 개수는 변하지 않고 배열만 달라지기 때문에 전체 질량은 일정하게 유지됩니다.
4. 일정 성분비 법칙: 완벽한 레시피
프루스트가 제안한 이 법칙은 화합물을 구성하는 성분 원소 사이에는 항상 일정한 질량비가 성립한다는 원리입니다.
토스트 비유 (Source 핵심): 완벽한 토스트 1개를 만드는 레시피가 '식빵 2장 + 달걀 1개'라고 합시다. 만약 식빵이 6장 있고 달걀이 4개 있다면, 토스트는 최대 3개까지만 만들어지고 달걀 1개는 남게 됩니다. 화합물도 이처럼 원자들이 제멋대로 섞이는 것이 아니라 정해진 비율로만 결합합니다.
산화 구리(II) 생성의 질량비
구리(Cu)가 산소(O)와 결합하여 산화 구리(II)(CuO)가 될 때, 그 질량비는 다음과 같습니다.
구리 : 산소 : 산화 구리(II) = 4 : 1 : 5
5. 기체 반응 법칙: 부피의 정수비
게이뤼삭의 법칙에 따르면 온도와 압력이 같을 때 반응하는 기체와 생성되는 기체의 부피 사이에는 간단한 정수비가 성립합니다.
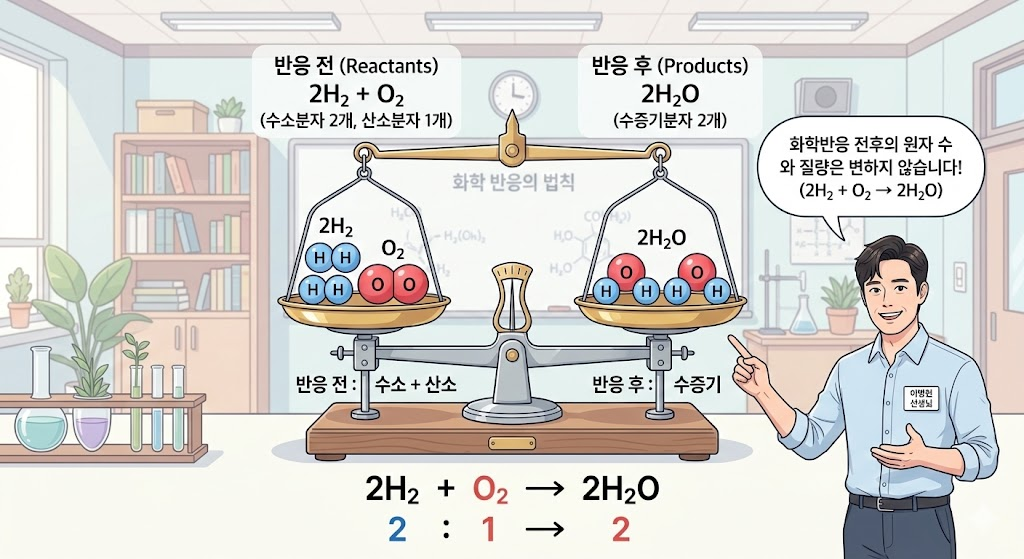
- 💧 수증기 생성 반응: 수소(2) + 산소(1) → 수증기(2)
→ 부피비 = 2 : 1 : 2 - ☁️ 암모니아 생성 반응: 질소(1) + 수소(3) → 암모니아(2)
→ 부피비 = 1 : 3 : 2
이 법칙의 가장 중요한 포인트는 부피비 = 화학 반응식의 계수비 = 분자 수의 비가 모두 일치한다는 점입니다. (질량비와는 관계없음에 유의하세요!)
6. 에너지 출입: 발열 반응과 흡열 반응
화학 반응이 일어날 때는 반드시 에너지(열)가 방출되거나 흡수됩니다.
- 🔥 발열 반응: 에너지를 방출하여 주변 온도가 높아지는 반응입니다.
- ❄️ 흡열 반응: 에너지를 흡수하여 주변 온도가 낮아지는 반응입니다.
실생활 속 에너지 출입 리스트
- 휴대용 핫팩 (철의 산화 반응 - 발열)
- 나무의 연소 및 산과 염기의 반응 (발열)
- 발열 도시락 (산화 칼슘과 물의 반응 - 발열)
- 질산 암모늄 냉찜질팩 (질산 암모늄과 물의 반응 - 흡열)
- 광합성 (빛에너지 흡수 - 흡열)
- 물의 전기 분해 및 소금과 물의 반응 (흡열)
자주 묻는 질문 (FAQ)
Q1. 기체가 발생하는 반응에서도 질량이 보존되나요?
Q2. 물리 변화인 '얼음이 녹는 현상'에서도 질량이 보존되나요?
Q3. 일정 성분비 법칙이 혼합물에서 성립하지 않는 이유는?
Q4. 부피비와 질량비는 왜 다른가요?
Q5. 나무를 태우고 남은 재의 질량은 왜 더 가벼운가요?
Q6. 광합성은 에너지를 어떻게 이용하나요?
💡 학습 포인트: "화학 반응 전후에 원자는 사라지거나 생기지 않고, 오직 재배열될 뿐이다!" - 이 핵심 문장을 꼭 기억하세요.
'교육 > 과학' 카테고리의 다른 글
| [중3 과학] 복사 평형과 지구온난화 정리 (1) | 2026.03.11 |
|---|---|
| 지구를 지키는 4개의 공기층, 기권의 층상 구조 완벽 정리 (0) | 2026.03.10 |
| 중3 과학 화학반응의 규칙과 에너지 변화 (0) | 2026.03.08 |
| 중3과학 물리 변화 vs 화학 변화 완벽 정리 (0) | 2026.03.07 |
| ☀️ 태양의 구조와 특징 (1) | 2026.01.20 |